
Il sistema periodico degli elementi è una disposizione che rappresenta gli elementi chimici. Di solito il sistema periodico di elementi è organizzato in forma tabulare.
La disposizione del sistema periodico degli elementi si basa su numeri atomici, configurazioni elettroniche e proprietà chimiche.
Quanto segue è la disposizione del sistema periodico di elementi:
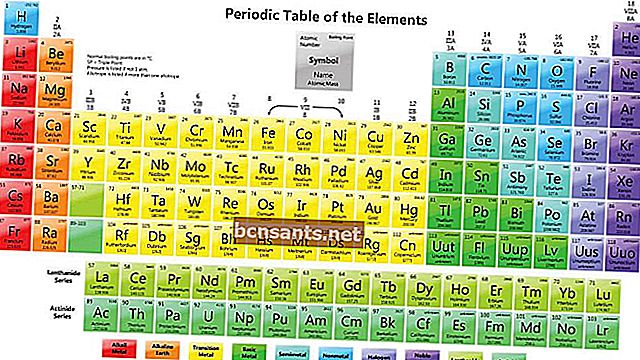
Come leggere gli elementi nel sistema periodico degli elementi
In SPU, troverai la scrittura di ogni elemento come mostrato di seguito.
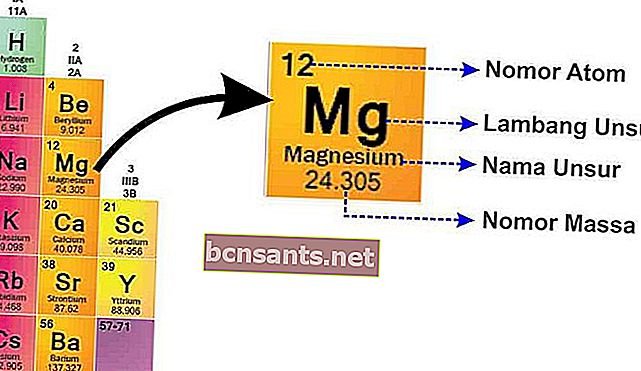
Da questa immagine si può spiegare:
- Numero di Massa
Il numero di massa è il nucleo dell'atomo che ha una carica positiva perché ci sono protoni che sono caricati positivamentee neutroni neutri
- Numero atomico
Il numero atomico ti dice il numero di protoni, perché l'atomo è neutro, il numero atomico ti dice anche il numero di elettroni .
Raggruppamenti di elementi
Nel sistema periodico di elementi, ogni elemento è raggruppato di conseguenza
- Gruppo
I gruppi si trovano nella colonna verticale della tavola periodica di sistema degli elementi. Gli elementi che si trovano nello stesso gruppo avranno la stessa configurazione elettronica di valenza.

- Periodo
I periodi sono gli elementi che si trovano in una riga orizzontale nella tavola periodica degli elementi di sistema. Il periodo mostra l'energia di ionizzazione , il raggio atomico, l'affinità elettronica e l' elettronegatività.

- Bloccare
Un blocco rappresenta una raccolta di elementi che hanno la stessa sottostruttura di elettroni di valenza.

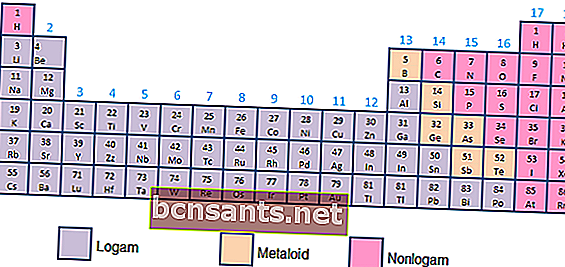
- Metalli, metalloidi e non metalli
In base alle proprietà chimiche e fisiche, gli elementi possono essere classificati come metalli (alta conduttività), metalloidi (conduttività tra metalli e non metalli) o non metalli (non aventi proprietà di conduttività, sotto forma di gas).
Energia di ionizzazione, raggio atomico, affinità elettronica ed elettronegatività
L'energia di ionizzazione, il raggio atomico, l'affinità elettronica e l'elettronegatività possono essere visti in base ai periodi e ai gruppi di elementi nel sistema elementare.
Leggi anche: Come identificate i corpi delle vittime di incidenti aerei?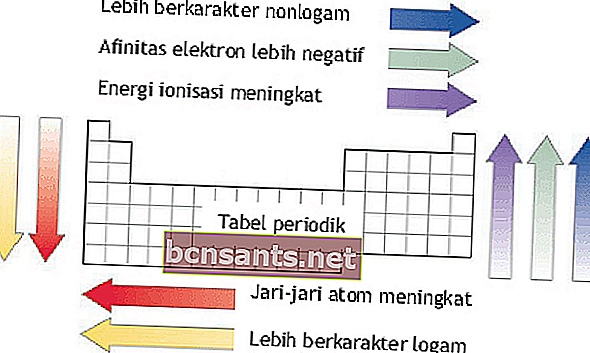
Energia ionizzata
L'energia di ionizzazione è l'energia richiesta per rimuovere uno degli elettroni esterni da un atomo allo stato gassoso.
In un periodo, l'energia di ionizzazione aumenta da sinistra a destra all'aumentare del numero atomico.
All'interno di un gruppo, le energie di ionizzazione diminuiscono dall'alto verso il basso all'aumentare del numero atomico.
Raggio atomico
Il raggio atomico è la distanza del nucleo atomico dalla traiettoria più esterna dell'atomo.
In un periodo, il raggio atomico aumenta dall'alto verso il basso.
All'interno di un gruppo, il raggio atomico aumenta da destra a sinistra.
Affinità elettronica
L'affinità elettronica è l'energia rilasciata da un atomo nel suo stato gassoso per formare ioni negativi.
In un periodo, l'affinità elettronica aumenta dal basso verso l'alto. All'interno di un gruppo, l'affinità elettronica aumenta da sinistra a destra.
Elettronegatività
L'elettronegatività è il valore della tendenza di un atomo ad attrarre elettroni nella formazione di legami chimici. Questa proprietà è importante nella formazione dei legami tra gli atomi.
In un periodo, l'elettronegatività aumenta dal basso verso l'alto.
In un periodo, l'elettronegatività aumenta da sinistra a destra.
Riferimento
- Tavola periodica degli elementi
- //www.studiobelajar.com/sistem-periodic-elements/
